PLoS Pathog:抗碳水化合物抗体2G12交叉中和HIV-1和H3N2病毒,有望作为对抗有包膜RNA病毒的通用抗体
来源:本站原创 2021-04-08 10:12
2021年4月8日讯/生物谷BIOON/---从HIV-1感染者身上发现的广泛中和抗体(bnAb)有助于设计和开发HIV-1候选疫苗和药物。其中的许多抗体已经显示出对不同HIV-1毒株和亚型的显著效力和广度。其中的一类不寻常的bnAb是专门靶向HIV-1包膜糖蛋白(Env)上的聚糖屏障(glycan shield)的抗碳水化合物抗体。虽然HIV-1 Env上
2021年4月8日讯/生物谷BIOON/---从HIV-1感染者身上发现的广泛中和抗体(bnAb)有助于设计和开发HIV-1候选疫苗和药物。其中的许多抗体已经显示出对抗不同HIV-1毒株和亚型的显著效力和广度。其中的一类不寻常的bnAb是专门靶向HIV-1包膜糖蛋白(Env)上的聚糖屏障(glycan shield)的抗碳水化合物抗体。虽然HIV-1 Env上的聚糖屏障起到了保护性屏障的作用,防止或阻碍了体液免疫系统对HIV-1 Env的免疫原性蛋白表面的识别,但与宿主蛋白相比,HIV-1上过于密集的聚糖屏障导致聚糖本身如今也被抗体靶向。这类抗碳水化合物抗体在对抗其他病毒病原体时很少见。
HIV-1不是唯一发生高度糖基化的病毒性病原体。自1968年引起流感大流行以来,人类季节性H3N2流感病毒由于其主要表面抗原血凝素(HA)上N-糖基化位点的积累,逐渐变得更加高度糖基化。这些新获得的N-糖基化位点主要位于HA球状头部的受体结合结构域(RBD)上,其中HA球状头部包含主要的抗原位点。N-连接聚糖可以帮助掩盖或重新定义表位,导致抗原漂移。HA中的聚糖和蛋白成分的不间断的抗原漂移使得每年都要更新季节性流感疫苗。然而以往的研究表明,HA表面上积累的加工程度较低的寡聚甘露糖聚糖(oligomannose glycan)可能是甘露糖结合凝集素的靶点,从而促进体外和体内的病毒抑制。
因此,这些聚糖修饰提出了一个问题,即抗碳水化合物抗体如今是否可以中和人类季节性H3N2流感病毒。抗碳水化合物抗体2G12是最早被发现的少数针对HIV-1的中和抗体之一,是从HIV-1患者的混合血清中分离出来的。2G12通过与Env的gp120表面上的高甘露糖聚糖簇(mannose patch, 甘露糖斑)结合,在一个如今称为N332/ V3表位的位点附近中和HIV-1。2G12是极其不寻常的,它在它的两个Fab臂的重链可变区之间形成了一个结构域交换的二聚体,因此,它可以与gp120表面上多达4个不同的位于高甘露糖苷末端的Manα1-2Man二糖结合,而不会与氨基酸发生任何可观察到的接触。
在一项新的研究中,来自美国、英国和中国台湾的研究人员证实2G12在过去三十年中具有中和人类季节性H3N2病毒的能力,并通过对病毒天然HA蛋白和重组HA蛋白上的N-连接聚糖的结构生物学分析、质谱分析和进化分析来研究中和机制。在HA受体结合位点(RBS)附近的一个保守性的高甘露糖N-连接糖基化位点和一个新获得的高甘露糖N-连接糖基化位点都有助于2G12对流感病毒的这种广泛中和活性。相关研究结果近期发表在PLoS Pathogens期刊上,论文标题为“A cross-neutralizing antibody between HIV-1 and influenza virus”。

添加、去除或替换聚糖屏障的N-糖基化位点是RNA病毒逃避抗体识别的常用策略之一。在这项新的研究中,这些作者证明了2G12尽管作为抗HIV抗体被发现,但也具有广泛中和过去50年发生进化的人H3N2流感病毒的能力。通过全面的和基于进化轨迹的位点特异性糖蛋白组学、突变和负染色电子显微镜(nsEM)成像,他们发现2G12中和H3N2流感病毒是通过与存在于N-糖基化位点N165和N246上的两个高甘露糖聚糖结合实现的,其中这两个位点位于HA受体结合位点的近端。由此看来,2G12很可能代表了一种针对人类流感病毒的中和抗体,它只识别HA表面上的聚糖表位。1980年前后N246的出现使得H3N2流感病毒在N246和N165处赋予了可以被2G12识别的寡甘露糖聚糖簇。那么,这些位点的逃逸突变体很可能具有较高的适应成本,这是因为,保守性N165的破坏会降低病毒的适应能力,而N246位点的破坏在近期的病毒中无法得到拯救。
病毒的天然抗原与可溶性重组蛋白的糖基化谱相似度如何,是疫苗设计的重要问题之一。比如,已经发现可溶性重组HIV-1 Env和病毒天然HIV-1 Env的糖型(glycoform)存在一些差异,可能会影响bnAb的中和和诱导。从这些作者对H3N2流感病毒的数据来看,来自293F细胞的重组HA和来自MDCK-SIAT1细胞(过度表达α-2,6-连接的唾液酸受体的Madin-Darby犬肾细胞)的病毒HA之间的位点特异性高甘露糖聚糖是保守的。这一发现也提示着可溶性重组HA可以作为免疫原,以试图促进抗碳水化合物抗体产生。
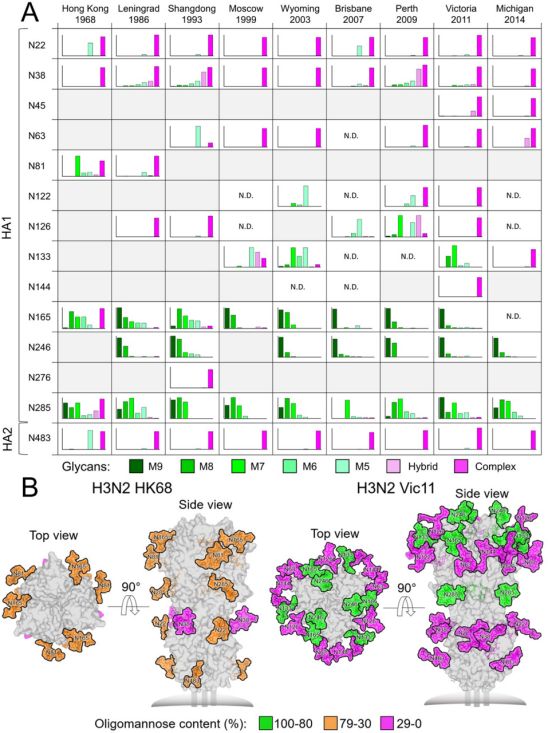
H3N2 HA糖蛋白的位点特异性N -连接糖基化及充分糖基化的HK68 HA和Vic11 HA的模型。图片来自PLoS Pathogens, 2021, doi:10.1371/journal.ppat.1009407。
虽然自身聚糖的免疫原性较差,但如果在病毒糖蛋白上的密度足够高,它们可以通过抗体与糖链和蛋白相互作用而成为免疫反应的焦点。与高甘露糖聚糖的多价结合有助于2G12强效中和HIV-1。值得注意的是,2G12通过结合构成高甘露糖聚糖斑的4个主要N-糖基化位点,表现出对敏感HIV-1病毒株的中和作用。在这项新的研究中,2G12通过靶向仅由两个N-糖基化位点形成的甘露糖聚糖簇,仅在亚微摩尔IC50下中和敏感的H3N2流感病毒毒株,与bnAb CR9114相比,效力低了5~10倍。与HIV-1 Env相比,HA三聚体内的高甘露糖N-糖基化位点较少,似乎造成了这种效力差异。
2G12的不完全中和可能是其他附近的N-糖基化位点(N133,N285)分散了它的中和能力。这种聚糖组成的异质性也会导致不完全中和,特别是对于2G12来说,除了高甘露糖聚糖存在异质性之外,还存在复合聚糖。在以前的一项研究中,在低浓度(0.5 mM)的Man7、Man8和Man9的情况下,2G12与gp120的结合对Man9和Man8来说几乎相同,对Man7来说较少(约20%)。在几种抗HIV-1的抗体中也发现了不完全中和的现象,可能是由于聚糖异质性造成的。
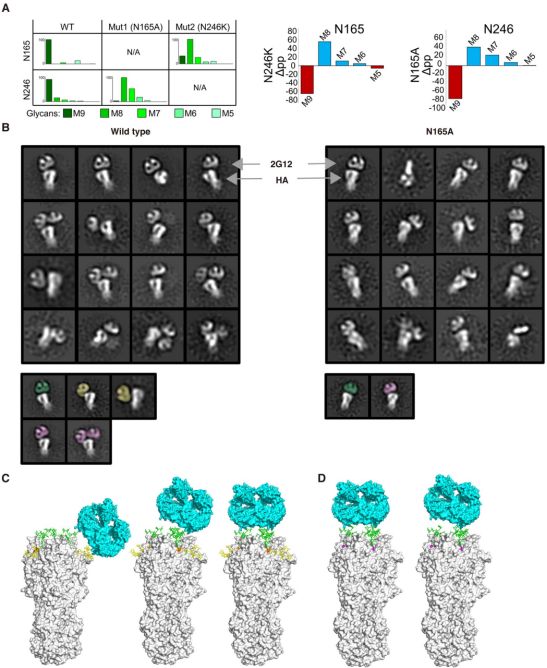
在N165和N246和2G12的糖型结合模式下与HA野生型和聚糖突变体结合。图片来自PLoS Pathogens, 2021, doi:10.1371/journal.ppat.1009407。
由于通常没有发现流感病毒HA诱导的2G12样抗体(即类似于2G12的抗体),这似乎表明HA上的甘露糖聚糖簇还没有成为免疫选择压力的焦点。许多有包膜病毒病原体,如埃博拉病毒、丙型肝炎病毒、拉沙热病毒和冠状病毒(包括SARS CoV-2)都是高度糖基化的,在其表面抗原上呈现寡聚甘露糖。
事实上,除了H3N2 HA和HIV-1 Env之外,2G12被认为可以通过识别S2亚基上的高甘露糖聚糖来结合SARS-CoV-2的刺突蛋白(S蛋白)。表面抗原上的甘露糖聚糖簇也可以被各种凝集素识别或捕获,如人甘露糖结合凝集素(MBL)或DC-SIGN。与这些作者在H3 HA受体结合位点附近发现高甘露糖聚糖相似,在拉沙病毒的糖蛋白受体结合位点附近也发现一些高甘露糖聚糖。根据这些作者的发现,存在于高糖基化病毒的关键功能位点附近的其他高甘露糖聚糖簇有可能是2G12的靶点。此外,最近从未感染HIV-1的人群中分离出2G12样的Fab二聚化聚糖反应性抗体。在感染了猿-人类免疫缺陷病毒(simian-human immunodeficiency virus, SHIV)的恒河猴中也发现了这类聚糖反应性抗体,而且Fab二聚化聚糖反应性抗体前体分子也可通过疫苗接种来增强。因此,没有结构域交换的2G12样抗碳水化合物抗体确实可以通过接种疫苗引起。
在这项新的研究中,这些作者揭示了2G12可以中和人类H3N2病毒,这是因为自从1968年大流行以来的H3N2进化过程中,大约30-35年前出现了N246糖基化位点。由于2G12也与HIV-1 Env上的高甘露糖表位结合,这就提出了这样的碳水化合物是否可以作为有包膜RNA病毒表面上的通用表位的问题。迄今为止,大多数针对表位有碳水化合物的病毒的抗体都是在HIV-1慢性感染的患者中发现的。虽然在HIV-1未感染的人类受试者中发现了2G12样Fab二聚化聚糖抗体和前体分子,但进一步的疫苗接种研究将阐明如何诱发2G12样抗碳水化合物抗体来对抗高糖基化的病毒。(生物谷 Bioon.com)
参考资料:
Chang-Chun D. Lee et al. A cross-neutralizing antibody between HIV-1 and influenza virus. PLoS Pathogens, 2021, doi:10.1371/journal.ppat.1009407.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


