Science:揭示超强效的合成纳米抗体中和新冠病毒机制
来源:本站原创 2020-11-19 21:12
2020年11月19日讯/生物谷BIOON/---在过去的20年里,有三种人畜共患的β冠状病毒进入人类群体,引起严重的呼吸道症状,死亡率很高。COVID-19大流行是由SARS-CoV-2引起的,SARS-CoV-2是这三种冠状病毒中最容易传播的一种。到目前为止,还没有针对任何冠状病毒的预防治疗方法获得批准,而且针对SARS-CoV-2的有效和广泛可用的疫苗
2020年11月19日讯/生物谷BIOON/---在过去的20年里,有三种人畜共患的β冠状病毒进入人类群体,引起严重的呼吸道症状,死亡率很高。COVID-19大流行是由SARS-CoV-2引起的,SARS-CoV-2是这三种冠状病毒中最容易传播的一种。到目前为止,还没有针对任何冠状病毒的预防性治疗方法获得批准,而且针对SARS-CoV-2的有效且广泛可用的疫苗的上市时间表仍然不确定。因此,开发新的治疗和预防方法仍然是至关重要的。
冠状病毒的病毒颗粒被含有负责病毒进入宿主细胞的同源三聚体跨膜糖蛋白---刺突蛋白(S蛋白)---的膜包围。S蛋白的表面暴露部分由两个结构域---S1和S2---组成。S1结合宿主细胞受体血管紧张素转化酶2(ACE2),而S2催化病毒和宿主细胞膜的融合。
包含在S1内的是受体结合结构域(RBD)和N末端结构域(NTD),其中RBD直接与ACE2结合。RBD通过一个柔远的区域连接到S蛋白的主体,并且可以以一种不可访问的向下构象(down-state)或一种可访问的向上构象(up-state)存在。与ACE2结合需要RBD处于向上构象,并使得它可被宿主蛋白酶裂解,从而触发病毒进入宿主细胞所需的S2构象变化。在SARS-CoV-2病毒颗粒中,S蛋白在一种活跃的开放构象(至少有一个RBD处于向上构象)与一种非活跃的封闭构象(所有三个RBD处于向下构象)之间进行交换。
在一项新的研究中,来自美国加州大学旧金山分校等研究机构的研究人员通过筛选酵母表面展示文库(含有大于2×109种合成纳米抗体序列)中与S蛋白胞外结构域(ectodomain)结合的纳米抗体序列,分离出中和SARS-CoV-2的单域抗体(纳米抗体)。
这些作者利用SARS-CoV-2 S蛋白的一种突变形式(SpikeS2P)作为抗原。SpikeS2P缺乏S1和S2结构域之间的两个蛋白切割位点之一,并引入两个突变和一个三聚化结构域(trimerization domain)来稳定S蛋白的融合前构象。他们用生物素或用荧光染料标记SpikeS2P,并通过多轮筛选---先是通过磁珠结合随后通过荧光活化细胞分选---来选择展示纳米体的酵母(图1A)。相关研究结果近期发表在Science期刊上,论文标题为“An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike ”。
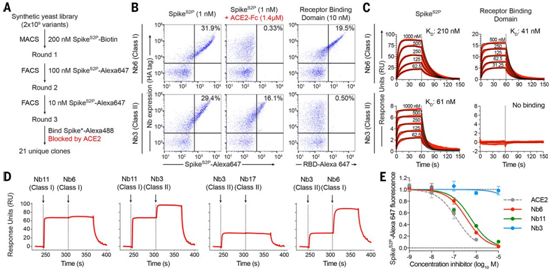
三轮筛选产生了21个独特的结合SpikeS2P的纳米抗体,而且ACE2胞外结构域(ACE2-Fc)的二聚体构造体可降低这种结合。这些纳米抗体分为两类。第I类纳米抗体结合RBD并直接与ACE2-Fc竞争(图1B)。这一类的典型例子是纳米抗体Nb6,它可与SpikeS2P和RBD单独结合,结合常数KD分别为210nM和41nM(图1C)。第II类纳米抗体,以纳米抗体Nb3为例,它结合SpikeS2P (KD=61nM),但不显示与RBD单独结合。在存在过量ACE2-Fc的情况下,Nb6和其他I类纳米抗体的结合完全被阻断,而Nb3和其他II类纳米抗体的结合则适度下降(图1B)。这些结果表明,I类纳米抗体以RBD为靶点阻断ACE2结合,而II类纳米抗体以其他表位为靶点。事实上,表面等离子共振(SPR)实验表明I类和II类纳米抗体可以同时结合SpikeS2P(图1D)。
与SpikeS2P相比,I类纳米体与分离的RBD的结合呈现出一致更快的结合速率常数(ka),这表明RBD可访问性影响了KD。接下来,这些作者测试了I类和II类纳米抗体抑制荧光标记的SpikeS2P与表达ACE2的HEK293细胞结合的效率(图1E)。I类纳米抗体Nb6和Nb11作为两个最有效的克隆出现,IC50值分别为370和540nM。II类纳米抗体在该试验中几乎没有表现出活性。他们优先选择了两种I类纳米抗体:Nb6和Nb11,它们强劲地结合SpikeS2P,与SpikeS2P或RBD结合之间的ka差异相对较小。对于II类纳米抗体,他们优先考虑Nb3,这是基于它在纯化过程中较高的相对产量。
阻止SARS-CoV-2进入宿主细胞的策略旨在阻断ACE2-RBD的相互作用。虽然高亲和力的单克隆抗体作为潜在的治疗方法处于领先地位,但是它们通过哺乳动物细胞表达产生的成本很高,并且需要由医疗保健专业人员进行静脉注射。预防性使用需要大剂量,这是因为只有一小部分抗体能穿过气道内的上皮细胞层。相比之下,纳米抗体可以廉价地在细菌或酵母中产生。纳米抗体固有的稳定性使得它们能够直接气雾化递送到鼻腔和肺部上皮。事实上,靶向呼吸道合胞病毒的三聚体纳米抗体(ALX-0171)的气溶胶递送最近被证明可以有效地降低住院婴儿的可测量病毒载量。最后,骆驼衍生纳米抗体的潜在免疫原性可以通过既定的人源化策略来降低。
纳米抗体多聚体化已被证明可以通过亲合力(avidity)来提高靶标亲和力(affinity)。针对Nb6和mNb6而言,结构指导设计的多聚体构造体同时结合S蛋白的所有三个RBD,可导致它们的效力显著提高。此外,鉴于RBD必须处于向上构象才能与ACE2结合,因此对RBD可访问性的构象控制可作为一种附加的中和机制发挥作用。事实上,当mNb6三聚体(mNb6-tri)与S蛋白结合时,它通过直接封闭结合位点和将RBD锁定在非活性构象来阻止ACE2结合。
II类中和纳米抗体展示了一种破坏S蛋白功能的潜在新机制。在预防或治疗性鸡尾酒中配对使用I类和II类纳米抗体可能强效地中和和阻止SARS-CoV-2的逃逸变体。因此,这些作者筛选出的抗S蛋白纳米抗体的组合稳定性、有效性和多样化的表位结合为限制COVID-19大流行造成的持续死亡提供了一种独特的潜在预防和治疗策略。(生物谷 Bioon.com)
参考资料:
Michael Schoof et al. An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike. Science, 2020, doi:10.1126/science.abe3255.
冠状病毒的病毒颗粒被含有负责病毒进入宿主细胞的同源三聚体跨膜糖蛋白---刺突蛋白(S蛋白)---的膜包围。S蛋白的表面暴露部分由两个结构域---S1和S2---组成。S1结合宿主细胞受体血管紧张素转化酶2(ACE2),而S2催化病毒和宿主细胞膜的融合。
包含在S1内的是受体结合结构域(RBD)和N末端结构域(NTD),其中RBD直接与ACE2结合。RBD通过一个柔远的区域连接到S蛋白的主体,并且可以以一种不可访问的向下构象(down-state)或一种可访问的向上构象(up-state)存在。与ACE2结合需要RBD处于向上构象,并使得它可被宿主蛋白酶裂解,从而触发病毒进入宿主细胞所需的S2构象变化。在SARS-CoV-2病毒颗粒中,S蛋白在一种活跃的开放构象(至少有一个RBD处于向上构象)与一种非活跃的封闭构象(所有三个RBD处于向下构象)之间进行交换。
在一项新的研究中,来自美国加州大学旧金山分校等研究机构的研究人员通过筛选酵母表面展示文库(含有大于2×109种合成纳米抗体序列)中与S蛋白胞外结构域(ectodomain)结合的纳米抗体序列,分离出中和SARS-CoV-2的单域抗体(纳米抗体)。
这些作者利用SARS-CoV-2 S蛋白的一种突变形式(SpikeS2P)作为抗原。SpikeS2P缺乏S1和S2结构域之间的两个蛋白切割位点之一,并引入两个突变和一个三聚化结构域(trimerization domain)来稳定S蛋白的融合前构象。他们用生物素或用荧光染料标记SpikeS2P,并通过多轮筛选---先是通过磁珠结合随后通过荧光活化细胞分选---来选择展示纳米体的酵母(图1A)。相关研究结果近期发表在Science期刊上,论文标题为“An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike ”。

图1.发现两种不同类别的抗S蛋白纳米抗体。图片来自Science, 2020, doi:10.1126/science.abe3255。
三轮筛选产生了21个独特的结合SpikeS2P的纳米抗体,而且ACE2胞外结构域(ACE2-Fc)的二聚体构造体可降低这种结合。这些纳米抗体分为两类。第I类纳米抗体结合RBD并直接与ACE2-Fc竞争(图1B)。这一类的典型例子是纳米抗体Nb6,它可与SpikeS2P和RBD单独结合,结合常数KD分别为210nM和41nM(图1C)。第II类纳米抗体,以纳米抗体Nb3为例,它结合SpikeS2P (KD=61nM),但不显示与RBD单独结合。在存在过量ACE2-Fc的情况下,Nb6和其他I类纳米抗体的结合完全被阻断,而Nb3和其他II类纳米抗体的结合则适度下降(图1B)。这些结果表明,I类纳米抗体以RBD为靶点阻断ACE2结合,而II类纳米抗体以其他表位为靶点。事实上,表面等离子共振(SPR)实验表明I类和II类纳米抗体可以同时结合SpikeS2P(图1D)。
与SpikeS2P相比,I类纳米体与分离的RBD的结合呈现出一致更快的结合速率常数(ka),这表明RBD可访问性影响了KD。接下来,这些作者测试了I类和II类纳米抗体抑制荧光标记的SpikeS2P与表达ACE2的HEK293细胞结合的效率(图1E)。I类纳米抗体Nb6和Nb11作为两个最有效的克隆出现,IC50值分别为370和540nM。II类纳米抗体在该试验中几乎没有表现出活性。他们优先选择了两种I类纳米抗体:Nb6和Nb11,它们强劲地结合SpikeS2P,与SpikeS2P或RBD结合之间的ka差异相对较小。对于II类纳米抗体,他们优先考虑Nb3,这是基于它在纯化过程中较高的相对产量。
阻止SARS-CoV-2进入宿主细胞的策略旨在阻断ACE2-RBD的相互作用。虽然高亲和力的单克隆抗体作为潜在的治疗方法处于领先地位,但是它们通过哺乳动物细胞表达产生的成本很高,并且需要由医疗保健专业人员进行静脉注射。预防性使用需要大剂量,这是因为只有一小部分抗体能穿过气道内的上皮细胞层。相比之下,纳米抗体可以廉价地在细菌或酵母中产生。纳米抗体固有的稳定性使得它们能够直接气雾化递送到鼻腔和肺部上皮。事实上,靶向呼吸道合胞病毒的三聚体纳米抗体(ALX-0171)的气溶胶递送最近被证明可以有效地降低住院婴儿的可测量病毒载量。最后,骆驼衍生纳米抗体的潜在免疫原性可以通过既定的人源化策略来降低。
纳米抗体多聚体化已被证明可以通过亲合力(avidity)来提高靶标亲和力(affinity)。针对Nb6和mNb6而言,结构指导设计的多聚体构造体同时结合S蛋白的所有三个RBD,可导致它们的效力显著提高。此外,鉴于RBD必须处于向上构象才能与ACE2结合,因此对RBD可访问性的构象控制可作为一种附加的中和机制发挥作用。事实上,当mNb6三聚体(mNb6-tri)与S蛋白结合时,它通过直接封闭结合位点和将RBD锁定在非活性构象来阻止ACE2结合。
II类中和纳米抗体展示了一种破坏S蛋白功能的潜在新机制。在预防或治疗性鸡尾酒中配对使用I类和II类纳米抗体可能强效地中和和阻止SARS-CoV-2的逃逸变体。因此,这些作者筛选出的抗S蛋白纳米抗体的组合稳定性、有效性和多样化的表位结合为限制COVID-19大流行造成的持续死亡提供了一种独特的潜在预防和治疗策略。(生物谷 Bioon.com)
参考资料:
Michael Schoof et al. An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike. Science, 2020, doi:10.1126/science.abe3255.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


