Nat Med:捡了芝麻丢了西瓜?基因编辑婴儿携带的CCR5-∆32突变显著增加死亡率
来源:本站原创 2019-06-13 06:36
2019年6月13日讯/生物谷BIOON/---在一项新的研究中,来自美国加州大学伯克利分校的研究人员发现一名中国科学家在去年出生的一对双胞胎婴儿中试图引入的一种基因突变在表面上有助于这两名婴儿抵抗HIV病毒感染,但这也会与生命后期的死亡率增加21%存在关联性。相关研究结果发表在2019年6月的Nature Medicine期刊上,论文标题为“CCR5-∆32 is deleterio
2019年6月13日讯/生物谷BIOON/---在一项新的研究中,来自美国加州大学伯克利分校的研究人员发现一名中国科学家在去年出生的一对双胞胎婴儿中试图引入的一种基因突变在表面上有助于这两名婴儿抵抗HIV病毒感染,但这也会与生命后期的死亡率增加21%存在关联性。相关研究结果发表在2019年6月的Nature Medicine期刊上,论文标题为“CCR5-∆32 is deleterious in the homozygous state in humans”。
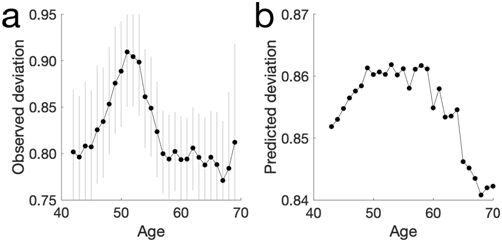
这些研究人员扫描了英国生物库(UK Biobank)中包含的40万多个基因组和相关健康记录,发现携带CCR5基因的两个突变拷贝的人在41~78岁之间的死亡率显著高于携带一个突变拷贝或没有携带突变拷贝的人。
以前的研究已将基因CCR5的两个突变拷贝与流感病毒感染后死亡率增加四倍相关联在一起,而且总体死亡率越高可能反映出因流感而死亡的可能性越大。但是,这些研究人员表示,可能有很多种解释,这是因为CCR5基因编码的蛋白参与很多人体功能,而且在那些同时在这个基因的两个拷贝上发生突变的人中,它不再发挥作用。
论文共同通讯作者、加州大学伯克利分校整合生物学教授Rasmus Nielsen说道,“除了与CRISPR婴儿有关的许多伦理问题之外,事实是,根据目前的知识,在不了解这种突变的全部作用的情况下,试图引入突变仍然是非常危险的。在这种情况下,它可能不是大多数人想要的突变。平均而言,这种突变实际上让你变得更糟糕。”
论文共同通讯作者、加州大学伯克利分校博士后研究员Xinzhu "April" Wei说道,“因为一个基因可以影响多个性状,而且,根据环境的不同,突变的影响可能会有很大的不同,我认为在任何生殖系编辑中都可能有许多不确定性和未知的影响。”
突变可阻止HIV感染
基因CCR5编码一种蛋白,该蛋白位于免疫细胞表面上,协助包括最常见的HIV毒株在内的一些病HIV毒株入侵并感染它们。去年11月,中国科学家贺建奎(Jiankui He)宣布他已经对至少两名婴儿进行了CCR5基因编辑试验,这一举动震惊了全世界,他说他想在这个基因中引入一种可以阻止HIV感染的突变。自然发生的让这种蛋白失活的突变在亚洲人中是罕见的,但是在大约11%的北欧人中发现的一种突变可以保护他们免受HIV感染。
这种基因突变,即Δ32(Delta 32),是指CCR5基因中缺失了一个长32个碱基对的片段。这种突变干扰了CCR5编码的这种蛋白在细胞表面上的定位,从而阻碍了HIV的结合和感染。贺建奎无法复制这种天然突变,不过似乎产生了类似的缺失,也会让这种蛋白失活。据报道,在这对双胞胎婴儿中,一个婴儿携带着一个接受CRISPR-Cas9基因编辑修饰的CCR5拷贝,而另一个婴儿的两个CCR5拷贝都接受了基因编辑。
然而,Nielsen表示,让一种在所有人类和大多数动物中发现的蛋白失活可能会产生负面影响,尤其是当这个基因的两个拷贝发生了所谓的纯合突变(homozygous mutation)时。
他说,“我们知道这是一种对有机体有影响的功能性蛋白,而且它在很多不同物种中都是非常保守的,因此平均而言,一种破坏这种蛋白的突变很可能对你不利。不然,进化机制很久以前就会破坏这种蛋白。”
在贺建奎的实验公开后,研究目前的遗传变异以了解人类、动物和植物性状起源的Nielsen和Wei决定使用来自英国生物库的数据来探究CCR5-Δ32突变的影响。这个数据库包含50万英国公民的与其医疗记录相关的基因组信息。这些基因组信息非常类似于从Ancestry.com网站和23andMe公司获得的信息:基因序列中近百万个个体变异---所谓的单核苷酸多态性(SNP)---的详细信息。
两项独立测量表明那些携带CCR5基因的两个突变拷贝的人具有较高的死亡率。在这个数据库中登记的携带两个突变拷贝的人数少于预期,这表明他们的死亡率高于一般人群。从40岁到78岁,携带两个突变拷贝的人的存活率低于预期。
Nielsen说,“登记前的这两种比例(即死亡率和存活率)和登记后的存活率都说明了同样的问题,这就是说,如果你有两个突变拷贝,你的存活率就会降低,而死亡率则会提高。拥有两个突变拷贝的人数明显不足。”
Nielsen说,鉴于Δ32突变在北欧人中相对较为常见,因此定是在某些时候受到自然选择的青睐,这很可能并不是为了阻止HIV感染,毕竟这种病毒仅自20世纪80年代以来才在人类中传播。
Wei说,有些证据表明这种突变与卒中发生后的存活率增加以及预防天花病毒和黄病毒--包括登革热病毒、寨卡病毒和西尼罗河病毒在内的一组病毒---感染有关。
这些研究人员表示,尽管存在这些可能的益处,但是成体体细胞和胚胎生殖细胞中产生基因突变的潜在意外影响仍然值得警惕。
Wei说,“我认为现阶段有很多关于基因功能的东西是未知的。就目前而言,将CRISPR技术用于生殖系编辑太危险了。”(生物谷 Bioon.com)
参考资料:
Xinzhu Wei et al. CCR5-∆32 is deleterious in the homozygous state in humans. Nature Medicine, 2019, doi:10.1038/s41591-019-0459-6.

图片来自Nature Medicine, 2019, doi:10.1038/s41591-019-0459-6。
这些研究人员扫描了英国生物库(UK Biobank)中包含的40万多个基因组和相关健康记录,发现携带CCR5基因的两个突变拷贝的人在41~78岁之间的死亡率显著高于携带一个突变拷贝或没有携带突变拷贝的人。
以前的研究已将基因CCR5的两个突变拷贝与流感病毒感染后死亡率增加四倍相关联在一起,而且总体死亡率越高可能反映出因流感而死亡的可能性越大。但是,这些研究人员表示,可能有很多种解释,这是因为CCR5基因编码的蛋白参与很多人体功能,而且在那些同时在这个基因的两个拷贝上发生突变的人中,它不再发挥作用。
论文共同通讯作者、加州大学伯克利分校整合生物学教授Rasmus Nielsen说道,“除了与CRISPR婴儿有关的许多伦理问题之外,事实是,根据目前的知识,在不了解这种突变的全部作用的情况下,试图引入突变仍然是非常危险的。在这种情况下,它可能不是大多数人想要的突变。平均而言,这种突变实际上让你变得更糟糕。”
论文共同通讯作者、加州大学伯克利分校博士后研究员Xinzhu "April" Wei说道,“因为一个基因可以影响多个性状,而且,根据环境的不同,突变的影响可能会有很大的不同,我认为在任何生殖系编辑中都可能有许多不确定性和未知的影响。”
突变可阻止HIV感染
基因CCR5编码一种蛋白,该蛋白位于免疫细胞表面上,协助包括最常见的HIV毒株在内的一些病HIV毒株入侵并感染它们。去年11月,中国科学家贺建奎(Jiankui He)宣布他已经对至少两名婴儿进行了CCR5基因编辑试验,这一举动震惊了全世界,他说他想在这个基因中引入一种可以阻止HIV感染的突变。自然发生的让这种蛋白失活的突变在亚洲人中是罕见的,但是在大约11%的北欧人中发现的一种突变可以保护他们免受HIV感染。
这种基因突变,即Δ32(Delta 32),是指CCR5基因中缺失了一个长32个碱基对的片段。这种突变干扰了CCR5编码的这种蛋白在细胞表面上的定位,从而阻碍了HIV的结合和感染。贺建奎无法复制这种天然突变,不过似乎产生了类似的缺失,也会让这种蛋白失活。据报道,在这对双胞胎婴儿中,一个婴儿携带着一个接受CRISPR-Cas9基因编辑修饰的CCR5拷贝,而另一个婴儿的两个CCR5拷贝都接受了基因编辑。
然而,Nielsen表示,让一种在所有人类和大多数动物中发现的蛋白失活可能会产生负面影响,尤其是当这个基因的两个拷贝发生了所谓的纯合突变(homozygous mutation)时。
他说,“我们知道这是一种对有机体有影响的功能性蛋白,而且它在很多不同物种中都是非常保守的,因此平均而言,一种破坏这种蛋白的突变很可能对你不利。不然,进化机制很久以前就会破坏这种蛋白。”
在贺建奎的实验公开后,研究目前的遗传变异以了解人类、动物和植物性状起源的Nielsen和Wei决定使用来自英国生物库的数据来探究CCR5-Δ32突变的影响。这个数据库包含50万英国公民的与其医疗记录相关的基因组信息。这些基因组信息非常类似于从Ancestry.com网站和23andMe公司获得的信息:基因序列中近百万个个体变异---所谓的单核苷酸多态性(SNP)---的详细信息。
两项独立测量表明那些携带CCR5基因的两个突变拷贝的人具有较高的死亡率。在这个数据库中登记的携带两个突变拷贝的人数少于预期,这表明他们的死亡率高于一般人群。从40岁到78岁,携带两个突变拷贝的人的存活率低于预期。
Nielsen说,“登记前的这两种比例(即死亡率和存活率)和登记后的存活率都说明了同样的问题,这就是说,如果你有两个突变拷贝,你的存活率就会降低,而死亡率则会提高。拥有两个突变拷贝的人数明显不足。”
Nielsen说,鉴于Δ32突变在北欧人中相对较为常见,因此定是在某些时候受到自然选择的青睐,这很可能并不是为了阻止HIV感染,毕竟这种病毒仅自20世纪80年代以来才在人类中传播。
Wei说,有些证据表明这种突变与卒中发生后的存活率增加以及预防天花病毒和黄病毒--包括登革热病毒、寨卡病毒和西尼罗河病毒在内的一组病毒---感染有关。
这些研究人员表示,尽管存在这些可能的益处,但是成体体细胞和胚胎生殖细胞中产生基因突变的潜在意外影响仍然值得警惕。
Wei说,“我认为现阶段有很多关于基因功能的东西是未知的。就目前而言,将CRISPR技术用于生殖系编辑太危险了。”(生物谷 Bioon.com)
参考资料:
Xinzhu Wei et al. CCR5-∆32 is deleterious in the homozygous state in humans. Nature Medicine, 2019, doi:10.1038/s41591-019-0459-6.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


